의료기기 자료관
닫기
품목갱신이란?
- 홈으로 이동
- 의료기기 자료관
- 품목갱신정보
- 품목갱신이란?
제도 목적
- 최초 허가·인증·신고 이후 안전성·유효성에 대한 주기적 재검토를 하고, 제조 또는 수입하지 않는 품목의 정리로 효율적인 의료기기 관리를 위해 5년마다 의료기기 갱신을 하고자 하는 것임
근거 법령
- 의료기기법 제49조, 같은 법 시행규칙 제62조 및 제62조의2
- 의료기기 제조허가등 갱신에 관한 규정
갱신 대상
- 허가ㆍ인증을 받거나 신고한 전(全) 등급 의료기기
- 단, 수출만을 목적으로 생산ㆍ수입되는 수출용 의료기기나, 조건부 허가ㆍ인증ㆍ신고 의료기기는 제외
갱신 신청기한
- 제조허가등의 유효기간이 끝나는 날의 270~ 180일 전까지 신청
갱신 기준
- 해당 의료기기의 안전성∙유효성에 중대한 문제가 없을 것
- 제조허가 등의 갱신에 필요한 자료를 성실히 제출할 것
- 해당 의료기기에 대한 생산 또는 수입실적이 있을 것
- 의료기기 관계 법령을 성실히 준수했을 것
- 그 밖에 위의 기준과 유사한 것으로서 식품의약품안전처장이 정하여 고시하는 기준에 부합할 것
갱신 신청 시 제출서류
- 해당 의료기기의 제조(수입) 허가증 또는 인증서 원본
- 이전 유효기간 동안 해당 의료기기의 안전성·유효성이 유지되고 있음을 입증하는 자료
- 이전 유효기간 동안 해당 의료기기의 생산 또는 수입 실적에 관한 자료
- 의료기기 관계 법령을 성실히 준수했을 것
- 이전 유효기간 동안 수집된 안전성 정보 및 조치에 관한 자료 등
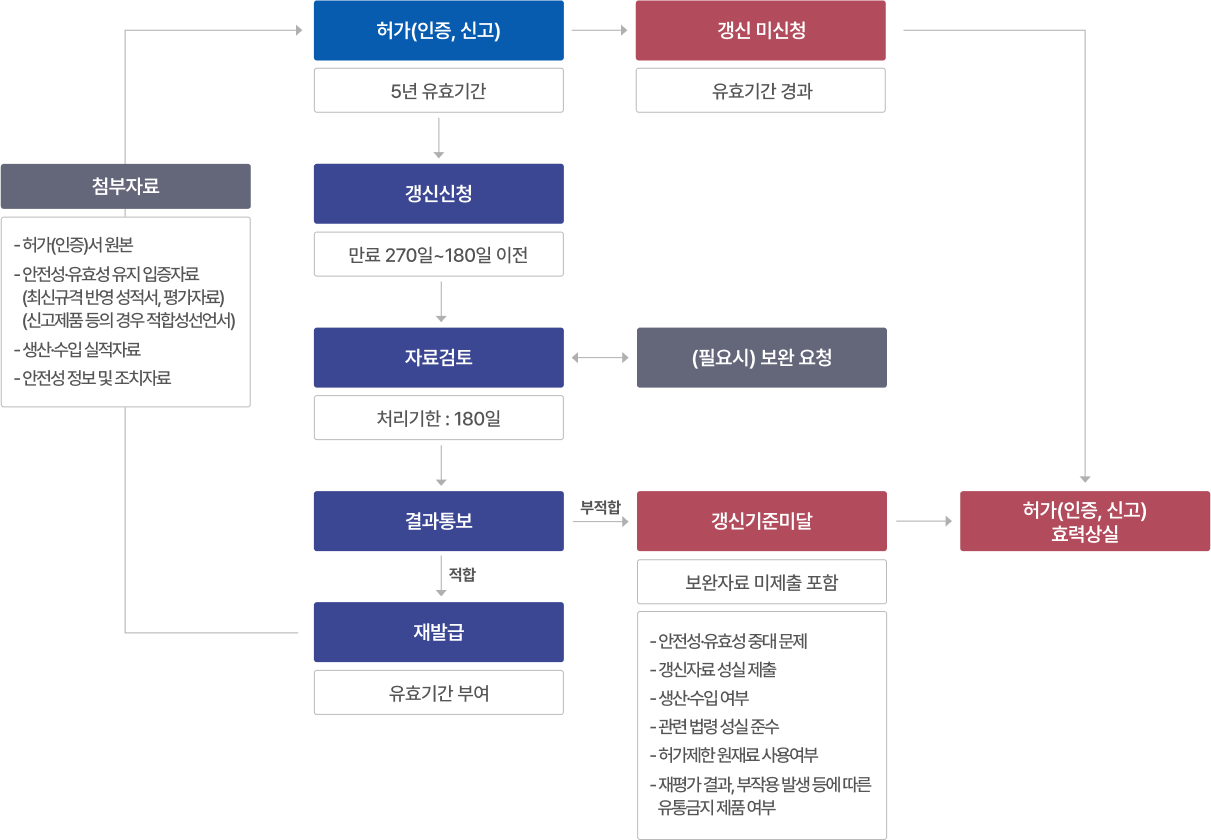
갱신 업무절차
[28159] 충청북도 청주시 흥덕구 오송읍 오송생명2로 187 오송보건의료행정타운 식품의약품안전처
[08389] 서울특별시 구로구 디지털로 30길 28, 마리오타워 102, 208, 303-1, 305호 한국의료기기안전정보원(운영)
Copyright © By Ministry of Food and Drug Safety. All rights reserved.






















